
국내 제약바이오 산업에서 연구개발(R&D) 활동이 본격화한 건 지난 1987년 물질특허가 도입되면서다. 이를 계기로 신약 개발의 중요성이 대두됐고 R&D는 제약바이오 기업들의 핵심 요소이자 미래 비전이 됐다. 글로벌 블록버스터급 신약에 거는 기대는 투자자들에게도 이어졌다. 하지만 핑크빛 미래를 꿈꿨던 투자자들의 피해가 잇따르면서 제약바이오 업종에 대한 신뢰도는 바닥을 치고 있다. 제약바이오 기업의 가치판단을 좌우하는 R&D에 대해 짚어본다. [편집자]
제약바이오 업종의 주가 흐름 부진이 장기화하면서 얼어붙은 투자심리도 좀처럼 회복하지 못하고 있다. 금리 인상에 따른 글로벌 경기 침체와 인플레이션 등의 영향도 있지만 반복된 기술이전(L/O) 계약 해지, 임상 실패, 허가자료 조작, 안전성 논란 등 계속된 악재가 제약바이오 업종에 대한 신뢰가 급감한 영향이 가장 크다. 이에 올해 제약바이오 업계의 L/O 이슈에도 주가 상승 폭은 미미한 수준에 그쳤다.
기술이전에도 주가 '부진'…상한가는 '에이비엘바이오' 유일
코오롱생명과학은 지난 4월 12일 장 마감 후 싱가포르의 주니퍼테라퓨틱스와 골관절염 유전자치료제 '인보사'를 최대 7234억원(선계약금 150억원) 규모에 달하는 기술수출 계약을 체결했다는 소식을 알렸다. 다음 날 회사의 주가는 전날 종가(3만7000원) 대비 최대 12.8%(4만1750원)까지 올랐지만 장 마감은 3만6700원으로 오히려 전날 종가보다 0.8% 하락했다.
앞서 지난 2018년 11월 19일 글로벌제약사 먼디파마에 6700억원(계약금 300억원) 규모로 기술이전했을 때 상한가를 기록한 것과는 대조적이다. 올해 기술이전 계약 체결에도 주가가 내린 배경은 주니퍼테라퓨틱스와의 기술이전과 동시에 먼디파마와의 기술이전 계약은 최종 해지된 영향이다.
보로노이도 지난 9월 13일 장 마감 후 미국의 메티스테라퓨틱스에 고형암을 타깃으로 한 인산화효소 저해 물질을 최대 6680억원(계약금 24억원) 규모로 기술이전했다고 공시했다. 다음날 주가는 최고 4만5250원(전날 종가 대비 18.8%)까지 올랐지만 종가는 3만9800원으로 전날보다 4.5% 상승하는 데 그쳤다.
티움바이오도 지난 8월 9일 중국 한소제약에 자궁내막증 신약후보물질 'TU2670'에 대한 중국 지역(중국, 대만, 홍콩, 마카오)의 전용실시권을 부여하는 기술이전 계약을 맺었다. 당일 주가는 전날 종가(1만8200원)보다 최대 8.8%까지(1만9800원)까지 올랐지만 장 마감 주가는 1만6600원으로 전날보다 8.8% 하락했다.
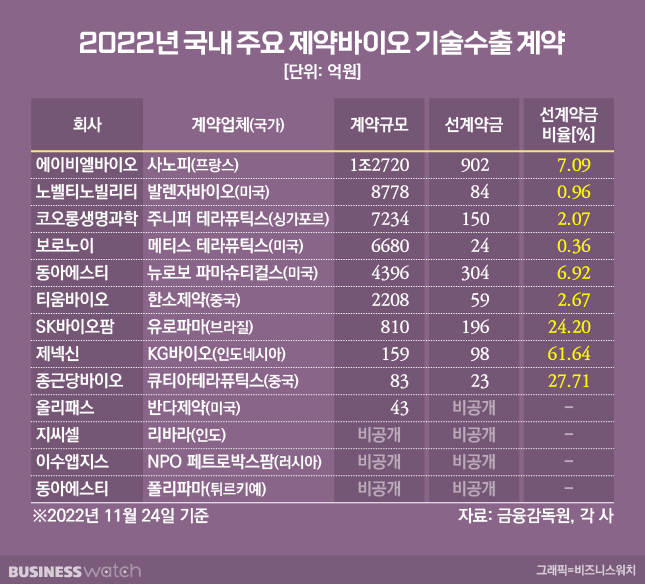
올해 L/O 소식으로 상한가를 기록한 건 이중항체 전문기업 에이비엘바이오가 유일하다. 에이비엘바이오는 파킨슨병 등 퇴행성뇌질환 치료 이중항체 후보물질 ABL301에 대해 사노피와 1최대 1조2720억원(계약금 900억원) 규모의 공동개발 및 기술이전 계약을 체결한 바 있다.
기업 가치판단은 '신약'…신약 가치판단은 '임상'
전문가들은 제약바이오 업종 투자심리 악화는 당분간 이어질 것으로 보고 있지만 내년에 R&D 모멘텀이 기대되는 신약들도 있는 만큼 투자심리 회복 가능성도 나오고 있다. 국가신약개발사업단에 따르면 현재 국내에서 개발 중인 신약 파이프라인은 1800여개에 달한다. 신약 파이프라인의 기술이전 가능성을 사전에 파악할 수는 없지만 신약 파이프라인의 가치판단을 할 수 있는 방법도 있다.
제약바이오는 다른 업종에 비해 투자 난이도가 높다. 일반적으로 기업의 재무제표와 현금흐름표를 통해 주가수익비율(PER)이나 주가순자산비율(PBR) 등을 따지며 기업의 가치를 측정한다. 하지만 제약바이오, 특히 바이오는 당장 현금흐름만 따졌을 때 투자 가치가 없는 곳이 대부분이다. 오직 비즈니스 모델로 기업의 가치와 성장성을 가늠해야 한다. 여기서 비즈니스 모델은 바로 '기술(신약)'이다.
여기서 가장 중요한 건 가짜 정보와 뉴스에 현혹되지 않아야 한다는 점이다. 결국 제약바이오 산업에 깊은 이해도가 요구되는데 연구 및 임상 결과 등에 대한 기업 발표를 곧이곧대로 받아들여서는 안 된다. 코로나 사태 당시 남양유업이 발표한 '유산균음료의 코로나 바이러스 억제 효과' 연구가 한 예다. 어떤 연구인지, 또 연구 대상과 결과 등을 세밀히 살펴볼 필요가 있다. [관련 기사: [기자수첩]불가리스 논란…"반도체 먹으면 천재되나"]
임상시험 디자인·결과·해석 주의 및 FDA 흐름도 글로벌 진출에 영향
가장 주의 깊게 살펴야 할 부분은 제약바이오 기업들의 임상시험 결과다. 신약 개발에서 가장 중요한 단계로 여겨지는 임상 2상에는 평가변수(평가지표)가 있다. 1차 평가변수는 임상에서 안전성과 유효성을 가장 분명하게 입증 및 도출할 수 있는 최적의 변수로 임상 디자인을 설정하고 2차 평가변수는 1차 평가변수 외에 추가적으로 확인하고자 하는 변수로 설정한다. 약물의 유효성 평가변수는 전체생존기간(OS)와 무진행생존기간(PFS), 객관적 반응률(ORR) 등으로 통계적 유의성을 판단한다. 임상 3상 진입 가능성에 있어 1차 평가변수의 OS 수치가 가장 중요하다.
그동안 국내 제약바이오 기업들이 1차 평가변수를 달성하지 못했음에도 '2차 평가변수에서 유의미한 결과를 확인했다'는 식으로 표현하는 경우가 있다. 이를 '성공'으로 오인해서는 안 된다. 2상에서 1차 평가변수를 달성해도 3상에 진입하지 못하는 경우도 있는 만큼 2차 평가변수로 3상에 진입할 가능성은 더 낮다.
미국 허가 가능성을 살펴보는 건 더욱 까다롭다. 미국 식품의약국(FDA) 허가와 관련해서는 FDA의 트렌드를 짚는 것도 필요하다. 과거 FDA는 지난 2019년 중국에서 임상시험을 주로 진행했던 베이진의 림프종 치료제 '브루킨사'를 허가한 바 있다. 하지만 FDA는 올해 초 글로벌 제약사 릴리가 중국 이노벤트바이오로직스로부터 도입한 PD-1 면역항암제 '신틸리맙'은 승인을 거부했다.
이유는 크게 세 가지로 △중국 단일 국가에서만 임상 실시 △대조군을 키트루다가 아닌 화학요법으로 설정 △1차 평가변수를 전체생존기간(OS)이 아닌 무진행생존기간(PFS)으로 설정 등이었다. 최근 FDA는 중국에서 임상이 집중된 신약을 허가하지 않는 분위기다. FDA 허가를 위해서는 아시아인에 국한되지 않고 다양한 인종으로 임상 대상을 구성했는지도 살펴봐야 한다는 얘기다.
"제약바이오, 단기 성과 기대한 무분별 투자 주의해야"
제약바이오 업종 투자는 언젠가부터 '투기'로 인식되기 시작했다. 단기간에 큰 이익을 보려는 개인투자자들의 관심이 제약바이오 업종에 몰리면서다. 이익을 실현한 투자자도 있겠지만 신약 안전성 논란, 기술이전 계약 해지, 임상 실패 등 악재로 주가가 급락하면서 투자 피해를 본 사람들이 대거 쏟아졌다.
제약바이오 업종에 대한 투자에 있어 제대로 된 이해 없이 무분별하게 투자를 진행할 경우 투자 피해는 계속될 수밖에 없다. 과거 신라젠을 신라호텔 계열사로 알고 있거나 현대바이오를 현대그룹 계열사로 알고 투자한 사람도 실제 있었다. 또 일부 투자자들에게서 부정적인 사실은 무조건 배척하고 비난하는 등 특정 바이오기업을 맹신하는 성향도 나타나고 있다. 이는 오롯이 자신이 감당해야 할 투자 손실로 이어지는 만큼 삼가야 한다.
업계 관계자는 "개인투자자들은 단기 성과를 기대하고 투자에 뛰어드는 경우가 많은데 제약바이오는 임상 단계별로 수년씩 소요되고 신약 개발에 걸리는 총 시간이 평균 10~15년에 달한다"면서 "제약바이오는 분명히 미래 성장 가능성이 있는 산업이지만 개인투자자들이 기업과 신약의 가치를 판단하기에는 어려운 분야"라고 말했다.



























