셀트리온의 두번째 바이오시밀러 '허쥬마'가 유럽과 미국 판매허가를 기다리고 있다. 유럽에서는 이르면 내년 1분기중 심사결과가 나올 것으로 예측된다. 셀트리온에 두달 앞서 유럽에 판매허가를 신청한 삼성바이오에피스의 온트루잔트가 지난 20일 허가를 받았다.
허쥬마의 미국 심사결과는 내년 상반기중 발표될 것으로 예상되고 있다. 다국적제약사 암젠-앨러간의 ABP980가 셀트리온과 비슷한 시기에 신청서를 접수해 놓고 결과를 기다리고 있다. 허쥬마의 오리지널의약품인 로슈의 허셉틴은 미국에서 2019년 2월 특허가 만료된다. 다만 특허 무력화 시도가 이뤄지고 있어 출시는 이 보다 앞당겨질 가능성도 제기되고 있다.
셀트리온의 세번째 바이오시밀러 '트룩시마'는 올해 2월 유럽에서 판매허가를 받고 6월 미국에 판매허가를 신청했다. 내년 하반기중 미국 심사결과가 나올 예정이다. 트룩시마의 오리지널의약품인 로슈의 리툭산은 내년 12월 미국에서 특허가 만료된다. 트룩시마가 미국에서 판매허가를 받을 경우 유럽에 이어 미국에서도 최초로 허가받은 리툭산 바이오시밀러가 된다. 다국적제약사 노바티스의 자회사 산도즈가 경쟁자다. 산도즈의 릭사톤(GP2013)은 지난 6월 유럽에서 시판허가를 받고 올해 9월 미국에 신청서를 접수했다.
셀트리온의 첫 바이오시밀러 램시마는 83개국에서 판매허가를 받았다. 2013년 8월 허가받은 유럽에선 TNF-a억제제시장의 40%를 점유하고 있다. 국가별로는 노르웨이 94%, 핀란드 89%, 네덜란드 66%, 영국 43% 등의 순이다. 셀트리온은 램시마의 오리지널의약품 레미케이드의 제조사 J&J와 벌인 물질특허 소송에서 지난해 8월 승소판결을 받으면서 미국에서도 바이오시밀러 시판을 앞당길 수 있었다.
램시마는 7년동안 2000억원을 투입해 탄생했다. 국내에 이어 2013년 8월 유럽에서 판매허가를 획득하면서 날개를 달았다. 유럽에서 첫 항체 바이오시밀러 판매허가였다. 셀트리온은 J&J의 레미케이드 유럽 허가가 풀리는 2015년 2월 판매에 돌입했다.
이어 미국을 비롯해 여러나라에서 판매허가를 얻어 지난해 램시마 매출이 7480억원을 기록했다. 이베스트투자증권 리서치센터는 계열사 셀트리온헬스케어가 판매하는 램시마 올해 매출이 8086억원, 2018년에는 1조1488억원에 이를 것으로 전망했다.
셀트리온은 시장에 안착한 램시마에 이어 허쥬마와 트룩시마 판매지역을 확대하고 이에 맞춰 생산설비를 증설하고 있다. 2019년까지 1공장을 증설해 생산능력을 19만리터로 늘리고 2021년까지 3공장을 완공해 생산능력을 31만리터로 확대한다는 계획이다. 3공장 건설 지역은 국내·외 가능성을 열고 검토중이다.

◇ 바이오시밀러 황무지 개척
셀트리온은 글로벌시장에서 바이오시밀러 개척자로 인정받고 있다.
국내에서 처음으로 바이오시밀러 사업 모델을 선보인 건 셀트리온이다. 해외에서도 2000년대말까지 관련 임상규정이 제대로 갖춰져 있지 않았다. 바이오시밀러라는 개념이 등장하기 전 세계 바이오의약품시장은 다국적제약사가 오리지널의약품 특허권을 토대로 독과점하는 구조였다. 이로 인해 비싼 약값은 대체 의약품을 쓸 수 없는 환자들에게 큰 부담이 됐다.
셀트리온은 이같은 구조를 바꿀 바이오시밀러시장을 주목했다. 또 2002년 2월 출범 당시부터 글로벌시장을 겨냥했다. 특히 미국에 비해 주요 바이오의약품의 특허만료가 빠른 유럽시장에 초점을 맞췄다.
셀트리온은 출범직후 미국 바이오기업 벡스젠과 손잡고 VCI(VaxGen-Celltrion Inc)를 설립해 바이오시밀러 사업에 필요한 자금과 기술, 영업망을 들여와 공장 설립에 나섰다. 2003년 3월 1공장을 시작으로 현재 14만리터 규모의 생산능력을 갖추게 됐다.
한때 미국발 글로벌 금융위기로 글로벌임상을 위한 자원조달에 어려움을 겪기도 했지만, 2008년 8월 기업공개 직후 투자자들의 주목을 받으며 사업에 탄력을 받기 시작했다. 셀트리온은 증시 상장 후 당시 4곳에 불과했던 코스닥 시가총액 1조클럽 반열에 들었고, 이듬해 허쥬마 글로벌임상에 착수했다.
2009년 8월 허쥬마, 2010년 3월 램시마에 대한 글로벌 임상1상을 시작해 각각 3년이 되지 않아 임상3상을 마쳤다. 두 품목의 임상은 세계 22개국 100개 지역에서 총 1400명이 넘는 환자를 대상으로 진행됐다.
◇ 종합독감항체신약 등 차세대 주자 주목
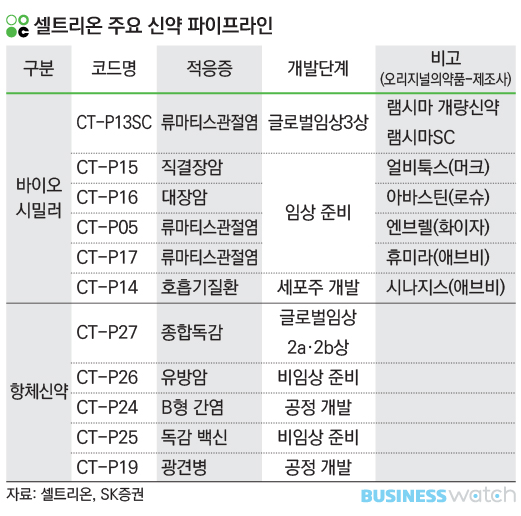
CT-P27은 각종 유행성, 계절성 인플루엔자에 약효를 보이는 종합 인플루엔자 항체치료제로, 칵테일 주사제 형태로 개발중이다. 현재까지 진행된 연구 결과 CT-P27은 시험관실험과 동물실험에서 유행·계절성 바이러스와 인간에게 전염된 적이 있는 조류매개 인플루엔자 대부분(H1, H2, H3, H5, H7 및 H9)에서 효과를 보이는 것으로 나타났다. 셀트리온은 영국에서 2014년 8월 임상2a상을 마치고 현재 글로벌 임상2a상 2b상을 동시 진행중이다.
램시마를 피하주사제 제형으로 개량한 램시마SC는 2019년 발매 목표로 개발중이다. 지난해 6월 글로벌 임상3상에 착수해 진행중이다. 이밖에 2019년 7월 미국과 2020년 1월 유럽에서 특허가 만료되는 로슈의 대장암 항암 바이오의약품 아바스틴의 바이오시밀러(CT-P16) 등 다양한 임상을 준비중이다.
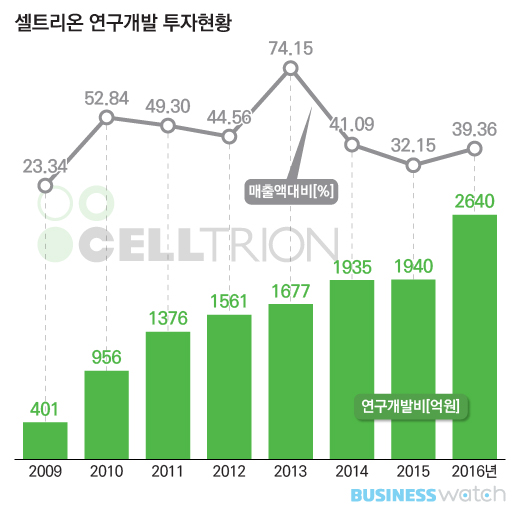
셀트리온은 매출의 4분의 1 가량을 연구개발에 투입한다. 올해 3분기까지는 매출대비 22.8% 수준인 1541억원을 연구개발비로 집행했다. 셀트리온 임직원 1193명중 절반 가량인 545명이 연구개발직이다.
셀트리온의 수익성이 대폭 개선되면서 연구개발 투자는 더 확대될 전망이다. 지난해 셀트리온은 영업이익률 43.7%를 기록했다. 같은 기간 국내 주요 제약사 평균 영업이익률8.03%를 크게 웃도는 수치다. 올해들어서는 3분기까지 누적 매출 5848억원으로 전년동기대비 26.7% 늘었고, 영업이익은 3678억원으로 106.5% 증가했다. SK증권은 셀트리온이 올해 매출 9390억원으로 전년동기대비 40% 늘고, 영업이익 5263억원으로 110.8% 증가할 것으로 전망했다.