
최근 HLB생명과학이 신주인수권부사채(BW) 일반공모 청약에서 흥행을 거뒀습니다. 모집금액인 407억원의 100배에 이르는 4조1079억원의 자금이 몰렸는데요. 경쟁률은 100대 1을 넘어섰습니다. 국내외 주식시장이 지지부진한 상황에서 HLB생명과학의 공모 흥행에 이목이 집중됐는데요. HLB생명과학이 이번 공모 청약에 성공할 수 있었던 요인에도 자연스럽게 시선이 쏠렸습니다.
HLB생명과학은 지난 2일 1000억원 규모의 공모 BW 발행을 결정했습니다. BW는 채권의 성격을 가지면서, 투자자가 원할 경우 사전에 정한 가격에 신주를 살 수 있는 권리(신주인수권증권)도 붙은 채권입니다. 사채의 만기일은 2025년 6월 15일로, 만기이자율은 2%가 적용됐고요. 전환가액은 1만1925원이었습니다. 다만 먼저 진행한 구주주 청약에선 59.27%의 다소 아쉬운 청약률을 기록했죠.
회사는 BW 발행으로 조달한 자금 중 400억원은 운영자금으로, 나머지 600억원은 타법인 인수자금으로 활용할 계획입니다. 앞서 지난달 말 HLB생명과학은 체외진단 의료기기업체 '에임'을 979억원에 인수한다고 발표한 바 있는데요. 979억원의 인수금액은 현금 529억원과 450억원 규모의 전환사채(CB) 발행을 통해 지불할 예정이라고 밝혔습니다. 즉 이번에 조달한 자금 600억원은 에임 인수에 투입될 것으로 보입니다.
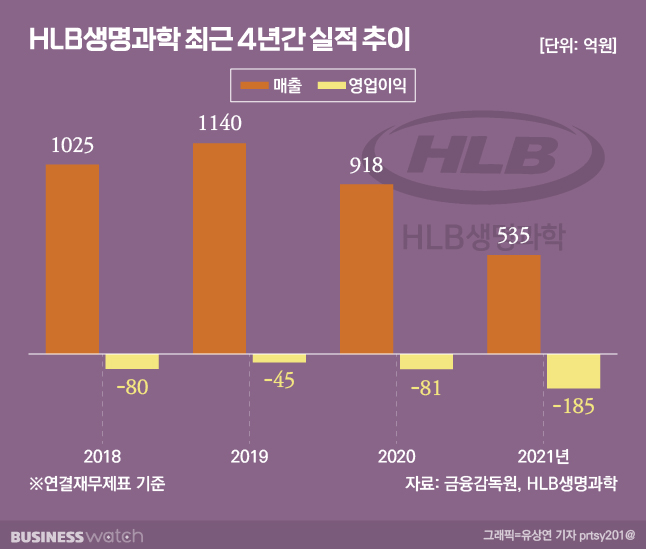
이번 BW 청약 흥행엔 HLB생명과학의 인수합병(M&A)에 대한 기대감이 반영됐다는 분석이 나옵니다. △재무구조 개선과 △현금창출원(캐시카우) 확보 두 가지 측면에선데요. HLB생명과학은 4년 연속 영업손실을 내고 있습니다. 연결기준 지난해 영업손실은 185억원으로 전년보다 적자 폭이 커졌습니다. 지난 4년간 누적 영업손실만 390억원에 달합니다.
반면 에임은 재무구조가 탄탄한 업체로 꼽힙니다. 진단 의료기기의 제품 생산을 위한 전체 공정 시스템을 갖췄고요. 한국애보트진단, 에스디바이오센서 등을 주요 고객사로 두고 있어 국내 유통망을 통한 수출 경쟁력도 갖고 있습니다. 지난해엔 감염증 예방과 진단에 필요한 의료기기를 제조·판매하면서 매출이 크게 뛰었습니다. 지난 2019년 77억원 수준이었던 매출은 지난해 1669억원까지 증가했습니다. 지난해 순이익은 342억원으로 전년보다 2배 이상 늘었습니다.
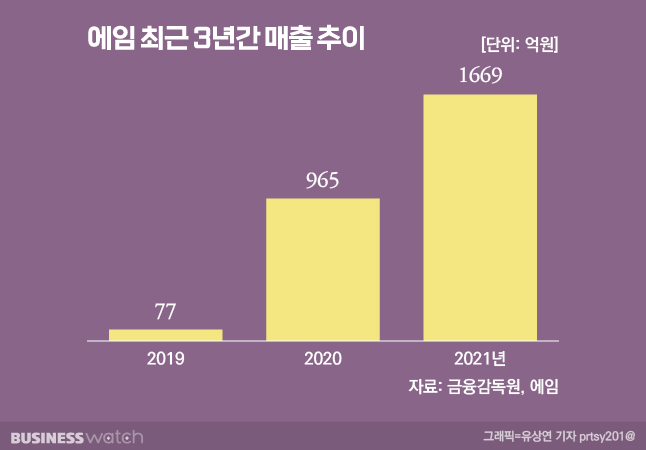
업계에선 에임 인수가 HLB생명과학의 재무구조 개선에 도움을 줄 것으로 보고 있습니다. 합병 절차가 마무리되면 오는 3분기부터 에임의 실적이 HLB생명과학의 실적에 반영됩니다. 실제 모회사인 HLB 역시 지난해 체외진단 의료기기업체 '에프에이'를 인수해 재무구조 개선 효과를 본 경험이 있고요. 에임을 통해 확보한 캐시카우를 바탕으로 연구개발(R&D) 자금을 자체적으로 조달하는 것도 가능해질 전망입니다. HLB생명과학은 지금까지 R&D 자금을 주로 CB를 발행해 조달해왔습니다.
여기에 항암신약 '리보세라닙'도 순항 중입니다. 리보세라닙은 혈관내피세포수용체(VEGFR-2)를 선택적으로 차단하는 먹는(경구용) 표적항암제입니다. 위암, 간암, 대장암, 선양낭성암 등 다양한 암종을 적응증으로 개발하고 있고요. HLB생명과학은 리보세라닙의 한국 판권과 일본 및 유럽지역의 일부 수익 권리를 보유하고 있습니다.
HLB는 최근 열린 미국임상종양학회(ASCO 2022)에서 리보세라닙 연구 결과를 대거 공개했는데요. 회사에 따르면 리보세라닙은 간암 1차 치료제 다국가 임상3상에서 통계적 유의성을 확보한 데 이어 선양낭성암 임상2상에서도 치료 효과를 입증했습니다. 특히 리보세라닙은 미국 식품의약국(FDA)으로부터 위암과 선양낭성암 치료제로 희귀의약품(ODD) 지정을 받았습니다. FDA 희귀의약품으로 지정되면 별도 심사를 거쳐 임상3상 없이 신약 품목허가 신청(NDA)을 할 수 있습니다.
회사 관계자는 "FDA 가속승인을 목표로 하고 있으며 올해 NDA 제출을 준비 중"이라고 설명했습니다. 선양낭성암의 경우 현재 방사선 치료나 수술을 제외하고 표준 치료제가 없는 만큼 가속승인에 큰 기대를 걸고 있는 분위긴데요. 가속승인을 받으면 간암 1차 치료제보다 신약 허가를 더 빠르게 받을 수 있다는 전망도 나옵니다. 간암 1차 치료제의 임상 전체 데이터는 오는 9월 열리는 유럽종양학회(ESMO)에서 공개할 계획입니다.
HLB생명과학은 최근 리보세라닙 외 파이프라인 강화에도 힘을 쏟고 있습니다. 회사는 그동안 파이프라인에서 리보세라닙 의존도가 지나치게 높다는 지적을 받아왔는데요. 유방암과 비소세포폐암 등을 적응증으로 하는 '파이로티닙' R&D에도 속도를 내는 모습입니다. 또한 리보세라닙의 적응증도 동물용 항암제와 노인성 황반변성 치료제로 확대하고 있고 신규 항암제 발굴에도 나서고 있습니다. HLB생명과학의 대담한 투자가 좋은 성과로 이어질지 관심이 모아집니다.

























