
한미약품의 신약 개발이 또 한 번 좌초될 위기입니다. 아테넥스사에 기술수출했던 경구용 항암신약 ‘오락솔’이 미국에서 시판허가 문턱을 넘지 못한 건데요. 올해 미국식품의약국(FDA)에서 시판허가가 날 것으로 기대를 모았지만 돌아온 것은 보완요구 서한(CRL, Complete Response Letter)이었습니다. 어떻게 된 일일까요?
오락솔은 한미약품의 ‘오라스커버리’ 플랫폼 기술이 적용된 항암 신약입니다. 오라스커버리는 파클리탁셀 성분의 주사용 항암제를 경구용으로 바꿀 수 있는 기술입니다. 오락솔은 여기에 경구흡수증진제 엔세키다(Encequidar)를 결합해 경구제의 단점으로 지적받아온 낮은 흡수율 문제도 개선했습니다.
기존의 주사형 파클리탁셀은 투약 전 필수적으로 스테로이드와 항히스타민제를 투여해야 하는 등 투약 때마다 병원을 방문해야 했습니다. 반면 오락솔은 간편하게 집에서 경구용 항암제만 복용하면 되는 겁니다. 개발에 성공하기만 하면 약 20조 원에 달하는 파클리탁셀 성분 항암제 시장을 뒤흔들 경쟁력을 갖추고 있었죠.
한미약품은 지난 2011년 12월 아테넥스에 4244만 달러(한화 약 487억 원) 규모로 기술이전하는데 성공했습니다. 아테넥스도 오락솔의 복용 편리성이 시장에서 충분히 경쟁력이 있다고 판단한 겁니다. 아테넥스는 수년간 임상을 진행하면서 유의미한 결과를 내놨습니다.
그 결과 오락솔은 지난해 FDA로부터 우선심사 대상으로 지정받기도 했는데요. 우선심사 대상은 효과 및 안전성의 유의미한 개선 가능성이 있는 의약품에 한해 신약 승인 여부를 6개월 내에 결정할 수 있도록 한 제도입니다. 일반 심사의 경우 통상 10개월이 소요됩니다. 오락솔이 FDA의 우선심사 대상이 되면서 허가에 대한 기대감은 높아졌습니다.
특히 아테넥스가 지난해 상업화를 위한 물밑작업을 활발하게 전개하면서 오락솔의 허가에 대한 기대감을 더욱 키웠습니다. 아네텍스는 지난해 미국의 투자자산운용사인 오크트리 캐피털 매니지먼트와 2억 2500만 달러(한화 약 2530억 원) 규모의 대출 계약을 체결했습니다. 1억 달러는 계약금 명목으로 즉각 지급받고 나머지 1억 2500만 달러는 FDA에서 '오락솔'의 허가를 획득한 후 조달받는 조건이었습니다.
또 캐나다의 헬스케어 전문 자산운용사 사가드 헬스케어 로열티 파트너스와도 5000만 달러(약 562억 원) 규모의 RIF(Revenue Interest Financing) 계약을 체결했습니다. 이 두 계약의 공통점은 '오락솔의 허가'가 전제라는 겁니다. 계약금은 오락솔의 공급 및 영업·마케팅 비용으로 투입될 예정이었습니다. 아테넥스는 지난해 오락솔의 중국 판권을 서브 라이센싱 아웃하면서 한미약품에 45억 원 규모의 마일스톤을 지급하기도 했습니다.
그러나 기대와는 달리 FDA로부터 돌아온 건 보완요구 서한이라는 통첩이었습니다. 경구용 항암제인 오락솔이 기존 정맥주사 대비 호중구 감소증 후유증에 대한 우려가 있기 때문입니다. FDA 서한에 따르면 오락솔의 시판허가를 위해서는 미국 내 전이성 유방암 환자 대상으로 적절한 신규 임상시험을 수행해 추가적인 안전성 데이터를 확보해야 합니다.
또 투여 용량 최적화 등 안전성을 개선할 수 있는 추가적 전략도 필요하다는 내용이 포함돼 있습니다. 오락솔이 미국 시판허가를 획득할 경우 한미약품이 수취할 수 있었던 2400만 달러(약 284억 원)의 기술료 수취도 기약 없이 미뤄지게 됐습니다.
서한 내용만 보면 자료를 보완해 다시 시판허가에 도전하면 될 것 같지만 그리 간단한 문제가 아닙니다. 신규 임상을 진행하기 위해서는 많은 시간과 자금이 더 필요합니다. 다행인 것은 아테넥스가 오락솔을 포기하지 않고 재도전할 의지가 있다는 겁니다. 앞서 올해 초 열린 JP모건 컨퍼런스에서 아테넥스는 오락솔의 빠른 시장 출시 및 정착을 위해 역량을 집중한다고 밝힌 바 있습니다. 이번 FDA 결정에 대해 임상시험 설계 및 범위를 논의하고 시판허가 승인 조율을 위한 미팅도 요청한다는 계획입니다.
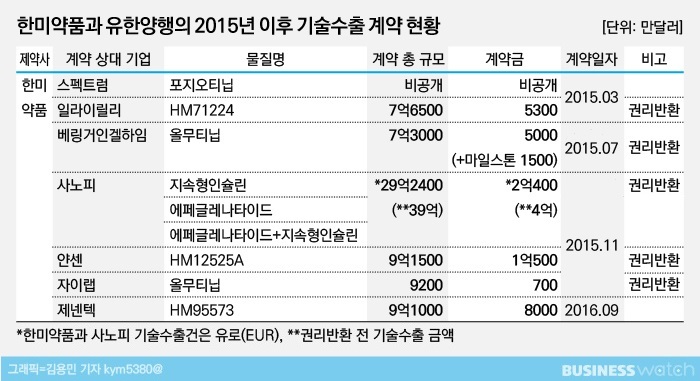
업계에서는 한미약품의 기술수출 성패에 대해 상반된 분석을 내놓고 있습니다. 한미약품이 기술수출했던 계약들이 줄줄이 파기되면서 기술수출 자체를 부정적으로 보는 시선도 나오고 있습니다. 지난 2015년 기술수출했던 총 9건의 계약 중 남은 건 항암신약 ‘포지오티닙’과 ‘벨바라페닙(HM95573)’ 2건과 2012년 기술수출한 호중구감소증 치료신약 ‘롤론티스’ 뿐입니다. 이 중 벨바라페닙의 경우 제넨텍에 라이선스 아웃한 지 수년이 지난 현재 글로벌 임상 진입을 앞두고 있습니다. 롤론티스는 평택 바이오신공장 실사가 무기한 연기 중입니다.[관련 기사: 신약 기술수출로 웃고 울고…'그 자체로 성과']
기술수출은 부족한 자금을 대신해 신약 개발을 이어갈 수 있다는 장점이 있습니다. 그러나 글로벌 제약사들이 도중에 개발을 포기한다면 해당 물질에 대한 신뢰도는 떨어지게 됩니다. 이후 자체 임상으로 변경하더라도 경쟁약물의 개발속도에 뒤쳐져 가치가 떨어질 수 있습니다. 개발단계나 진행속도 등을 통제하기 어렵기 때문에 기술수출이 오히려 신약 개발의 성공 가능성을 낮출 수 있다는 겁니다.
하지만 대부분의 기술수출 계약이 실패했다고 남아 있는 계약들도 실패하리라는 법은 없습니다. 업계가 포지오티닙과 롤론티스에 거는 기대는 여전합니다. 한미약품의 파트너사인 스펙트럼은 올 상반기 FDA에 포지오티닙의 신속승인 신청서를 제출할 예정입니다. 이르면 하반기 승인이 기대되고 있습니다.
롤론티스 역시 공장 실사 연기 이유가 코로나19 때문인만큼 부정적으로 해석하기는 어렵습니다. 한미약품은 FDA의 바이오공장 모의검사를 진행하는 등 준비를 모두 마치고 실사 일정이 잡히기만 기다리고 있습니다. 허가에 성공만 한다면 기술료와 판매에 따른 로열티가 보장됩니다. 한미약품은 실적 개선과 동시에 그동안의 불명예를 모두 씻어낼 수 있게 됩니다.
한미약품 창립자였던 고(故) 임성기 회장의 모토는 48년간 오직 ‘신약 개발을 통한 제약강국 건설’이었습니다. 지난해 임 회장은 타계했지만 한미약품은 올해도 신약 개발을 위한 외길을 걷고 있습니다. 임 회장 생전에 못 다한 ‘신약 개발을 통한 제약강국의 건설’을 한미약품이 이뤄낼 수 있을지 좀 더 지켜봐야겠습니다.

























