
삼성바이오에피스와 셀트리온이 글로벌 제약사 애브비의 자가면역질환 치료제 '휴미라' 바이오시밀러로 내년 미국 진출을 앞두면서 확전을 예고하고 있다. 삼성바이오에피스는 저농도와 고농도 제품 출시 준비를 마쳤고 셀트리온은 경쟁력 강화를 위해 오리지널 제품과 처방 없이 대체조제가 가능한 '상호교환성' 임상에 뛰어들었다.
삼성바이오에피스는 미국 현지 시각으로 지난 15일 미국식품의약국(FDA)으로부터 휴미라 바이오시밀러 '하드리마'(성분명 아달리무맙, 유럽 제품명 임랄디)의 고농도 제품인 100mg/mL이 허가를 획득했다고 18일 밝혔다.
하드리마는 류마티스 관절염, 소아 특발성 관절염, 건선 관절염, 강직성 척추염, 크론병, 궤양성 대장염 및 판상 건선 등의 치료제다. 회사는 지난 2019년 7월 FDA로부터 저농도 제품인 50mg/mL에 대한 허가를 획득한 바 있다.
아직 FDA 허가 심사 단계에 있는 셀트리온은 '상호교환성(interchangeability)'을 통해 경쟁력을 확보하는 전략을 세웠다. 셀트리온은 지난 1일 FDA에 휴미라 바이오시밀러인 '유플라이마'의 상호교환성 글로벌 3상 임상시험계획(IND)을 신청했다. 해당 임상계획은 지난 10일 미국국립보건원(NIH)에 등록됐는데 이는 FDA가 IND 승인을 했다는 의미다.
이에 따르면 셀트리온은 오는 11월 16일부터 임상에 들어갈 예정이며 연구 완료일은 오는 2024년 3월 29일로 예상된다. '상호교환성' 임상에 성공하면 오리지널 의약품과 대체 가능한 지위를 확보할 수 있어 처방 없이도 약국에서 구입이 가능해진다. 다만 셀트리온의 '유플라이마'는 지난 2020년 11월 FDA에 허가 신청을 제출했지만 아직 허가 승인은 나지 않은 상태다.
오리지널 의약품인 휴미라는 미국 애브비가 판매하고 있는 블록버스터 바이오의약품으로 지난해 전 세계에서 약 207억 달러(약 25조원)의 매출을 기록했다. 이 중 미국 매출이 173억 3000만달러(약 21조원)로 대부분을 차지하고 있다.
지난 2018 10월 유럽에서 휴미라의 핵심 특허가 만료되면서 바이오시밀러들이 대거 출시됐다. 삼성바이오에피스와 셀트리온도 유럽에서는 이미 휴미라 바이오시밀러 제품들을 출시한 상태다. 반면 가장 큰 시장인 미국에서는 물질특허 2개가 각각 내년 9월과 2024년 7월에 만료된다. 삼성바이오에피스와 셀트리온은 모두 애브비와 특허합의를 했기 때문에 7월 1일부터 미국에서 휴미라 바이오시밀러를 출시할 수 있다.
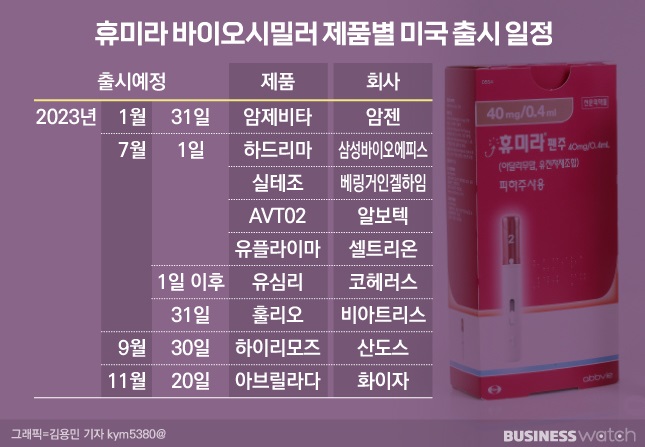
휴미라의 고농도 제형은 약물 투여량을 절반으로 줄일 수 있고 통증을 유발할 수 있는 구연산염을 제거한 것이 특징이다. 저농도 제품의 경우 주사를 여러 번 맞아야 하는 불편함이 있어 고농도 주사로 수요가 넘어가는 추세다. 이에 암젠, 베링거인겔하임, 비아트리스, 화이자, 알보텍 등 글로벌 기업들도 고농도 휴미라 바이오시밀러 개발에 나섰고 속속 허가를 받고 있다.
글로벌 기업들과 치열한 경쟁이 예상되지만 업계 기대는 밝다. 업계 관계자는 "미국의 휴미라 매출 21조원 중 10%만 가져와도 국내 상위 제약바이오 기업의 연매출 수준인 2조원에 달한다"면서 "특히 삼성바이오에피스와 셀트리온은 이미 미국 바이오시밀러 시장에 진출한 경험이 있어 휴미라 바이오시밀러의 시장 안착도 크게 어려움은 없을 것"이라고 말했다.



























