
삼성바이오로직스에 의약품 위탁개발(CDO) 서비스를 맡긴 국내 바이오텍(신약개발사)들이 임상시험 진입, 기술이전 등의 성과를 내고 있다. 특히 개발난이도가 높은 융합단백질 치료제의 세포주 및 공정개발 서비스를 받은 제약사들의 실적이 두드러진다.
유한양행의 자회사 프로젠은 최근 식품의약품안전처로부터 비만과 당뇨병 치료제로 개발 중인 후보물질 'PG-102'의 임상 2상 시험 허가를 받았다. PG-102는 GLP(글루카곤 유사 펩타이드)-1과 GLP-2에 동시에 결합하는 이중융합단백질 치료제다.
융합단백질은 두 개 이상의 단백질을 유전자재조합 방식으로 하나로 결합한 모달리티(약물이 약효를 내는 방법)다. 일반 단백질치료제와 비교해 강한 약효 등을 구현해 낼 수 있으나 복잡한 구조로 일관된 생산과 품질유지가 어려운 특징이 있다.
프로젠은 삼성바이오로직스와 PG-102를 생산하는 세포주를 개발했고 융합단백질 기준으로 당시 최고 수준인 4g/L의 생산성을 확보했다. 프로젠은 이를 통해 PG-102의 생산단가를 낮추고 '위고비', '젭바운드' 등 글로벌 비만약과 맞설 가격 경쟁력을 갖출 수 있게 됐다. 현재 PG-102의 생산성은 7g/L까지 개선된 상태다.
김종균 프로젠 대표는 "구조적 복합성이 높은 융합단백질로 4g/L의 생산성이 나오는 것은 당시 무척 놀라운 수준이었다"며 "현재 PG-102의 생산성을 극대화해 글로벌 비만약의 5분의 1 수준으로 가격 경쟁력을 확보할 수 있을 것으로 보고 있다"고 했다.
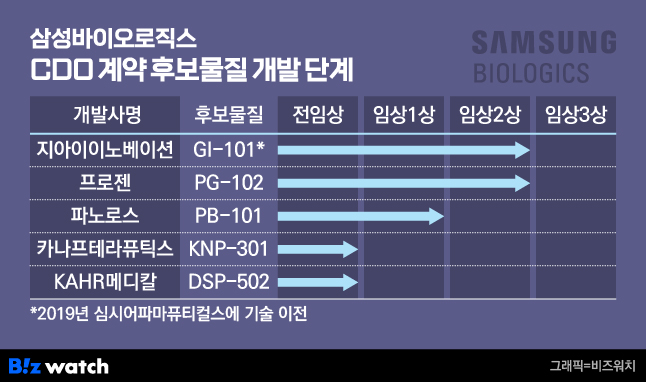
지아이이노베이션은 현재 면역항암제로 개발 중인 이중융합단백질 치료제 'GI-101' 및 'GI-101A(어드밴스드)'를 '키트루다(성분명 펨브롤리주맙)'와 병용투여하는 요법의 임상 1·2상 시험을 한국과 미국에서 진행하고 있다. 키트루다는 다국적 제약사 머크가 개발한 면역항암제다.
지아이이노베이션은 최근 삼성바이오로직스와 GI-101의 공정을 함께 개발해 약물의 반감기(약물의 성분이 체내에서 절반으로 줄어드는 데 걸리는 시간)와 약효 등을 개선했다. 지아이이노베이션은 새 공정으로 제조한 GI-101을 GI-101A로 이름 붙이고 미국 식품의약국(FDA)과 식약처에 새 임상시험 계획을 제출해 허가받았다.
지아이이노베이션은 지난 2018년 삼성바이오로직스와 처음 GI-101 세포주개발 등에 관한 CDO 계약을 맺었고 이듬해 이를 중국계 제약사 심시어파마슈티컬스에 7억9000만달러(1조900억원)에 기술이전한 바 있다.
장명호 지아이이노베이션 CSO(임상전략 총괄)은 지난해 열린 기자간담회에서 "GI-101의 제조 공정 변경을 통해 옛 공정과 비교해 3배 이상 높은 림프구 증식 효과를 확인했다"며 "다른 약물보다 월등히 높은 수준의 생산성도 확보했다"고 밝혔다.
이밖에 삼성바이오로직스와 융합단백질 CDO 계약을 맺은 국내 제약사로는 파노로스바이오사이언스와 카나프테라퓨틱스가 있으며 해외에서는 이스라엘계 제약사 KAHR메디칼 등이 있다.
파노로스바이오사이언스의 후보물질 'PB-101'은 현재 국내에서 임상 1상 시험 중에 있다. 카나프테라퓨틱스와 KAHR메디칼의 후보물질(KNP301, DSP502)은 전임상시험에서 우수한 약효를 확인하고 임상시험 진입을 준비 중이다.
삼성바이오로직스가 융합단백질 CDO 사업에서 우수한 성과를 낼 수 있었던 이유는 공정개발에 앞서 고객사의 융합단백질이 가진 물성을 파악하는 데 필요한 초기단계 플랫폼 기술을 구축했기 때문으로 분석된다.
삼성바이오로직스 관계자는 "항체와 달리 융합단백질은 다양한 API(활성의약품성분)에 항체의 결정화가능부위(Fc)를 융합하기 때문에 생산성, 순도, 안정성 등을 사전에 평가한 후 CMC(화학, 제조 및 품질관리) 공정에 들어갈 수 있다"며 "삼성바이오로직스는 '에스초지언트', '디벨롭픽'과 같은 CDO 플랫폼을 갖춰 이같은 평가가 가능하다"고 했다.
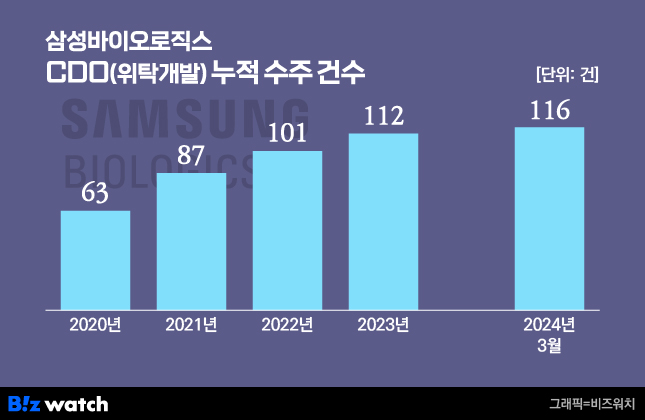
삼성바이오로직스는 지난 2018년 CDO 사업에 첫발을 내디뎠고 2022년 누적 수주 건수가 100건을 넘었다. 지난해 기준으로 삼성바이오로직스가 수행한 CDO 프로젝트에서 모달리티별로 차지하는 비중은 단일클론항체(60%), 이중항체(20%), 융합단백질(14%) 등의 순이다.
삼성바이오로직스의 CDO 서비스를 받은 고객사의 후보물질 중 현재까지 30개 이상이 임상시험계획(IND) 승인을 받았고 이 중 절반 이상이 미국, 유럽 등 글로벌 규제당국의 허가를 획득했다. 최근에는 리가켐바이오사이언스와 CDO 계약을 맺는 등 ADC(항체약물접합체)로 사업 영역을 넓히고 있다.
삼성바이오로직스의 CDO 서비스를 받았던 바이오텍 한 관계자는 "임상시험계획 승인뿐만 아니라 후보물질을 기술이전하는 데까지 삼성이 많은 도움을 줬다"며 "국내에 우수한 기술력과 시스템을 갖춘 곳이 있다는 것만으로 국내 바이오텍 성장에 큰 도움이 되는 게 사실"이라고 했다.

























