오는 2025년부터 2030년 사이 대형 블록버스터 의약품들의 특허가 줄줄이 만료됨에 따라, 글로벌 바이오 제약 시장의 판도 변화가 예고되고 있다. 특히 세계 최대 시장인 미국을 중심으로 바이오시밀러(바이오의약품 복제약) 기업들에게 거대한 기회의 문이 열릴 전망이다.
540조원 규모 시장 풀린다…특허 만료 러시
한국바이오협회 바이오경제연구센터가 24일 발표한 분석 보고서에 따르면, 2025년부터 2030년 사이 약 200개의 바이오의약품 특허가 만료될 것으로 보인다. 이 중 연 매출 10억 달러(약 1조3000억원) 이상의 '블록버스터' 급 의약품만 70개에 달한다.
지역별로는 미국에서 118개, 유럽에서 69개의 특허 보호가 종료될 예정이다. 이번 특허 만료로 영향을 받게 되는 매출 규모는 최소 2000억 달러에서 최대 4000억 달러(약 540조 원)에 이를 것으로 추산된다.
주목받는 블록버스터는 지난해 전세계 매출 1위 면역항암제인 '키트루다'로 2028년 미국 특허가 만료된다. 이 외에도 △옵디보(2028년) △오크레부스(2029년) △듀피젠트(2030년) 등 시장을 장악하고 있는 핵심 약물들이 대거 포함됐다.
센터는 이에 힘입어 2030년 글로벌 바이오시밀러 시장이 약 762억 달러(약 103조원) 규모까지 성장할 것으로 내다봤다.
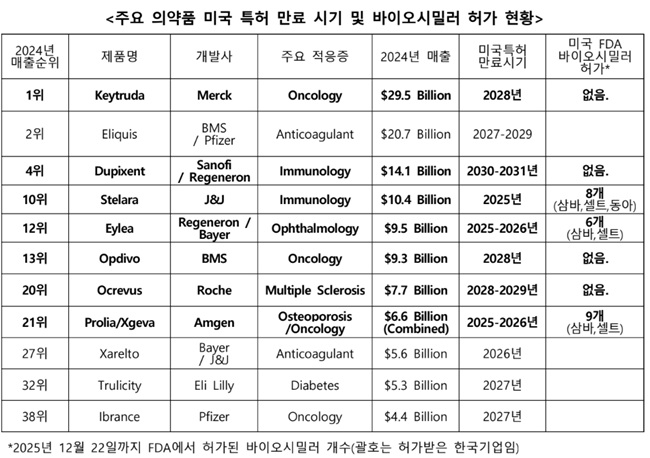
빅파마의 수성 전략 vs 바이오시밀러의 공세
특허 만료의 파괴력은 이미 '휴미라' 사례를 통해 증명된 바 있다. 자가면역질환 치료제인 휴미라는 독점권 상실 후 매출이 2022년 212억달러에서 2024년 90억달러로 반토막 났다.
위기를 느낀 글로벌 빅파마들은 '수명 연장' 전략에 총력을 기울이고 있다. 대표적으로 머크(MSD)는 키트루다의 특허 만료에 대비해 투약 편의성을 높인 피하주사(SC) 제형을 개발, 2025년 9월 FDA 승인을 획득하며 방어막을 쳤다.
그러나 바이오시밀러 기업들에게는 우호적인 환경이 조성되고 있다. 미국 식품의약국(FDA)와 유럽 의약품청(EMA)는 이르면 2026년부터 바이오시밀러 개발시 거쳐야 했던 '임상 3상(비교효능시험)'을 면제하거나 간소화하는 지침을 추진 중이다.
성공의 키워드… '가격·공급·유통'
규제 완화로 개발 비용과 기간이 줄어드는 것은 호재지만, 그만큼 신규 진입자가 늘어 경쟁은 더욱 치열해질 전망이다. 전문가들은 향후 바이오시밀러 시장의 성패가 단순한 기술력을 넘어 가격 경쟁력, 공급 안정성, 협상력등의 요소에서 갈릴 것으로 보고 있다.
업계 관계자는 "특허 절벽은 빅파마에게는 위기지만 준비된 시밀러 기업에게는 도약의 발판"이라며 "2026년 임상 3상 면제가 본격화되면 시장 진입 속도가 성패를 좌우하는 핵심 변수가 될 것"이라고 밝혔다.