보건당국이 국내·외 코로나19 치료제와 백신 개발 진행 상황에 대한 정보를 공유했다. 국내에서는 치료제 13건, 백신 2건의 임상이 진행 중이다.
식품의약품안전처는 국내·외에서 개발 중인 치료제 및 백신 등의 개발 진행 상황에 대한 정보를 제공한다고 26일 밝혔다.
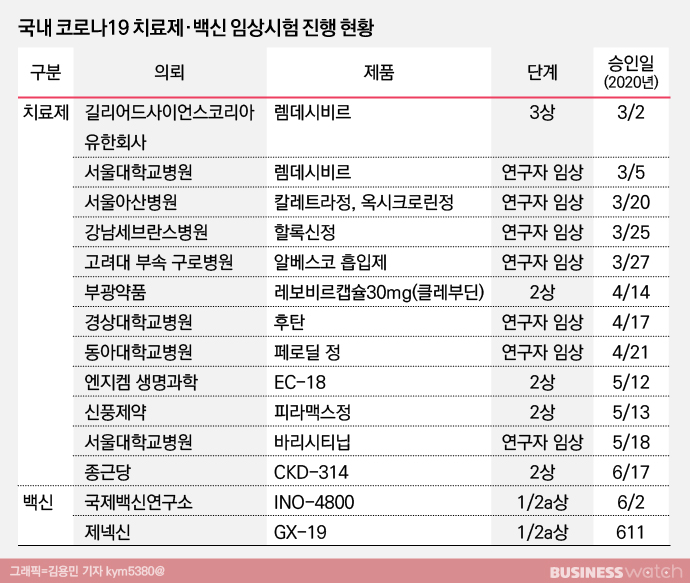
현재 국내에서는 치료제 13건, 백신 2건 등 총 15건의 임상시험이 승인됐다. 치료제 임상시험 13건을 개발 단계별로 살펴보면 ▲ 3상 임상시험 2건 ▲ 2상 임상시험 4건 ▲ 연구자 임상시험 7건이었다. 이중 우리나라에서 개발한 치료제로는 부광약품의 간염 치료제 '클레부딘', 신풍제약의 말라리아치료제 '피라맥스', 엔지켐생명과학의 ‘EC-18’, 종근당의 항응고제 '나파모스타트' 등이 모두 임상 2상을 진행 중이다.
의약품은 동물실험 단계인 전임상을 거친 후 사람에게 3단계에 걸쳐 안전성과 효과성을 확인한다. 먼저 1상의 경우 최초로 사람에게 투여해 안전성과 약동학 등을 평가하고, 2상에서 대상 환자들에게 투여해 치료효과를 탐색, 3상에서 더 많은 환자들에게 투여해 안전성과 치료효과를 최종적으로 확증해야 한다.
백신 임상시험은 2건 모두 초기 단계인 1상과 2상을 진행 중이며 이중 우리나라에서 개발 중인 백신은 제넥신의 ‘GX-19’가 1상과 2상을 동시에 진행하는 1/2상 단계에 있다.
국내 임상시험을 준비 중이거나 해외에서 임상 중인 코로나19 항체치료제로는 미국 ’L사‘가 임상시험을 진행하고 있으며, 류마티스관절염 치료제로 사용되고 있는 ’R사‘의 제품도 미국, 중국 등에서 임상을 진행하고 있다. 국내에서는 ’C’사가 임상시험 준비단계에 있다.
혈장치료제로는 G사가 완치된 환자의 혈장을 이용한 치료제를 개발하고 있으며, 현재 임상 2상을 준비 중이다.
현재 코로나19 예방을 위한 백신 중 현재 전 세계적으로 상용화된 제품은 없다. 해외에서는 영국 옥스퍼드 대학이 개발 중인 백신이 임상 2/3상 단계, 중국 C사와 미국 M사가 각각 개발 중인 백신이 임상 2상 단계, 그 외 12개 백신이 임상 1/2상 또는 1상 단계에 있다.
식약처는 렘데시비르와 함께 유력한 코로나19 치료제로 주목받았던 스테로이드제 ‘덱사메타손’, 항말라리아제 ‘히드록시클로르퀸’ 관련 치료정보도 공개했다. 앞서 영국 임상시험에서 '덱사메타손'이 중증환자의 사망률을 낮추는 데 효과가 있다고 발표된 바 있다. 이에 대해 식약처는 '덱사메타손'의 경우 면역억제 작용을 통해 치료 효과를 나타내는 것으로 급성호흡기증후군과 같은 중증 환자에 한정해 의사가 환자상태를 관찰하면서 투여하는 것이 적절할 것으로 보인다고 판단했다.
국내에서 덱사메타손은 원활하게 수급되고 있으며 정제 및 주사제 14개 품목이 생산 중이다. 정제는 연간 약 4300만 정, 주사제는 연간 약 6000만 앰플이 생산되고 있다.
'히드록시클로로퀸'의 경우 이달 국제보건기구(WHO)와 미국 국립보건원(NIH)에서 임상시험 자료를 분석한 결과, 환자에게 치료적 유익성이 인정되지 않는 것으로 판단되면서 관련 임상시험 중단을 각각 발표했다.
국내에서도 총 5건의 히드록시클로로퀸 임상시험이 승인됐다가 모두 조기 종료됐다.
식약처는 "코로나19 치료제·백신의 사용 및 개발 동향을 지속적으로 모니터링 해 나갈 것"이라며 "국내 품목허가 및 공급에 필요한 사항을 지원해 우리 국민의 치료 기회를 보장할 수 있도록 최선을 다할 계획이다"라고 말했다.