
또 다시 '의약품 불순물'이 수면 위로 떠올랐다. 정부는 원료의약품 등록제도(DMF)를 순차 시행하는 등 원료의약품 품질 강화에 나서고 있다. 업계에서는 근본적으로 원료의약품의 품질을 강화하기 위해서는 수입 의존도가 높은 원료의약품의 자급화를 확대해야 한다는 목소리가 높다.
하지만 국산 원료의약품은 수입 원료의약품 보다 단가가 높다. 복제의약품(제네릭)의 약가정책과 치열한 경쟁으로 기업들은 허리띠를 졸라매야 하는 상황이다. 원료의약품 품질 강화가 이뤄지기 위해서는 정부가 국산 원료의약품 자급화를 지원하는 등 정책 지원이 시급하다는 지적이다.
지난 9일 셀트리온제약, 현대약품 등 제약바이오 기업 36곳의 고혈압 치료제 73개 품목에서 불순물이 초과 검출됐다. 이에 따라 기업들이 자진 회수에 들어갔다. 이번에 불순물이 검출된 고혈압 치료제는 로사르탄, 발사르탄, 이르베사르탄 등 3종의 사르탄 성분에서 발견됐다. 앞서 지난 2018년도 고혈압 치료제에서 불순물이 발견된 바 있다.
첫 번째는 'N-니트로소디메틸아민(NDMA)'였다. 이번에는 약물 합성 시약인 아자이드 계열의 '아지도(AZBT)'다. 둘 다 기준치 초과시 암 유발 가능성이 있는 물질로 알려져 있다. 고혈압 치료제 외에도 2019년과 지난해에도 잇따라 위장약, 당뇨병치료제 등에서 기준치를 초과한 불순물이 발견돼 관련 제품들에 대한 판매중지 및 회수 조치가 이뤄졌다.
식품의약품안전처는 계속 불거지는 의약품 불순물 사태로 원료의약품 등록제도를 순차 개선하는 중이다. 식약처는 2017년 12월부터 신규 허가를 받는 제네릭의 DMF 등록을 의무화한 바 있다.
그러다 중국과 인도산 원료의약품에서 불순물이 검출되는 등 문제가 발생하면서 2019년 기존에 허가받은 의약품으로 대상을 확대하는 내용으로 법안을 개정했다. 이에 상용의약품은 올해 말까지, 고가의약품은 내년까지, '기타 의약품 및 생체를 이용하지 않은 시험이 필요한 의약품'은 오는 2023년 6월말까지 원료의약품을 등록해야 한다.
정부는 DMF에 공고된 제조원의 원료의약품만 사용하도록 해 의약품 품질 개선 및 수준이 강화될 것으로 기대하고 있다. 그러나 업계에서는 국산 원료의약품 사용을 확대해야 한다는 의견을 지속해 제기해왔다. 코로나 사태까지 불거지면서 중국과 인도에서 수입하던 원료의약품 공급에 차질이 생기면서 국산 원료의약품 자급화에 대한 목소리는 더욱 커졌다.
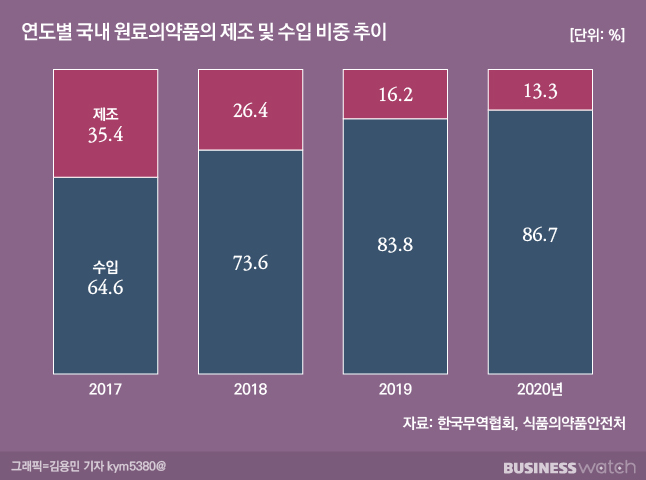
실제로 한국무역협회와 식품의약품안전처 등에 따르면 원료의약품 국내 자급률은 2017년 35.4%로 역대 최고치를 기록했다가 2018년 26.4%, 2019년 16.2%, 지난해 13.3% 등으로 급감했다. 원료의약품에 대한 수입 의존도가 높아 수급에도 문제가 생겼다. 유한양행, 현대약품, 신풍제약 등은 최근 수입 원료의약품의 수급 불안으로 일부 의약품들이 품절, 생산이 지연되고 있다.
결국 정부는 지난해 국산 원료의약품 사용에 대한 인센티브 방안으로 '신속심사' 카드를 꺼냈다. 세부 논의를 거쳐 이르면 내년부터 시행에 들어갈 예정이다.
하지만 업계 반응은 심드렁하다. 국내 제약바이오 기업들의 수입 원료의약품에 대한 의존도가 높은 것은 단가 때문이다. 국내에서 공장 가동 시 들어가는 인건비, 공정비 등 초기 비용이 수입하는 것보다 더 높다. 반면 의약품 가격은 지난해 제네릭 약가제도가 개편되면서 소수 품목들만 높은 가격을 받을 수 있도록 바뀌었다.
높은 약가를 받기 위해서는 오리지널 의약품과 동등하다는 것을 입증하는 생물학적 동등성 시험(생동성시험)과 등록된 원료의약품 사용 등 두 가지 요건을 충족해야 한다. 이 마저도 선착순 20개 제품까지만 해당된다. 등재 순서가 늦을수록 받을 수 있는 약가가 상한가에서 15%씩 낮아진다. 특히 과거에는 다수 기업들이 동일한 생동성시험 자료로 허가를 받을 수 있었지만 이제는 최대 4곳으로 제한된다. 기업별로 부담해야 하는 생동성시험 비용도 대폭 늘었다.
▷관련 기사: '1+3 제한' 본격 시행…제약업계 "기대 반 우려 반"(7월 29일)
높은 약가를 받을 수 있는 기업은 줄어든 반면, 제네릭 허가를 받기 위한 지출 비용은 더 커졌다. 원가가 높은 국산 원료의약품으로 전환할 경우 수익 감소는 물론 적자 위험도 있다. 이런 상황에서 '신속심사'로 국산 원료의약품 사용을 독려하겠다는 정부 정책은 국내 제약바이오 업계의 상황을 고려하지 못한 '탁상행정'이라는 지적이다.
업계 관계자는 "제네릭 허가 및 출시에 이전보다 더 많은 비용을 지출해야 하는 상황에서 국산 원료의약품을 사용할 경우 단가를 맞추기 어렵다"며 "국산 원료의약품 사용 시 세제 혜택이나 약가 보장 등의 금전적 인센티브가 필요하다"고 말했다.


























